Hallo Anonymous, falls du es eilig hast,
die Avogadro-Konstante  ist eine nach Amedeo Avogadro benannte physikalische Konstante, die als Teilchenzahl
ist eine nach Amedeo Avogadro benannte physikalische Konstante, die als Teilchenzahl 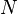 pro Stoffmenge
pro Stoffmenge  definiert ist:
definiert ist:

Sie gibt an, wie viele Teilchen (etwa Atome eines Elements oder Moleküle einer chemischen Verbindung) in einem Mol des jeweiligen Stoffes enthalten sind. Der aktuell empfohlene Wert[1] beträgt

also gut 602 Trilliarden Teilchen pro Mol.
Entsprechend der Definition der atomaren Masseneinheit  beträgt die Masse
beträgt die Masse 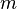 von 6,02214129 (27) ⋅ 1023 C-12-Atomen im Grundzustand exakt 12 g. Die molaren Massen aller anderen Stoffe werden auf C-12 bezogen.
von 6,02214129 (27) ⋅ 1023 C-12-Atomen im Grundzustand exakt 12 g. Die molaren Massen aller anderen Stoffe werden auf C-12 bezogen.
Aus Wikipedia.
Gruß asinus :- )